Politetrafloroetilen (politetrafloroetilen) çox güman ki, ən çox istifadə edilən flüoropolimerdir, çünki o, bir sıra xüsusiyyətlərə malikdir və onu geniş tətbiqlər üçün ideal material edir.Digər oxşar borulardan daha çevikdir və demək olar ki, bütün sənaye kimyəvi maddələrinə müqavimət göstərə bilər
Temperatur diapazonu floropolimerlər arasında ən geniş temperatur diapazonunu təmin edən təxminən -330°F ilə 500°F arasındadır.Bundan əlavə, əla elektrik xüsusiyyətlərinə və aşağı maqnit keçiriciliyinə malikdir.Ptfe boruları kimyəvi müqavimət və saflığın vacib olduğu ən çox istifadə edilən laboratoriya boruları və tətbiqləridir.PTFEçox aşağı sürtünmə əmsalına malikdir və məlum olan ən "sürüşkən" maddələrdən biridir
Xüsusiyyətləri:
100% təmiz PTFE qatranı
FEP, PFA, HP PFA, UHP PFA, ETFE, ECTFE, ən çevik floropolimer borularla müqayisədə
Kimyəvi cəhətdən inert, demək olar ki, bütün sənaye kimyəvi maddələrinə və həlledicilərə davamlıdır
Geniş temperatur diapazonu
Aşağı nüfuz
Hamar yapışmayan səth
Ən aşağı sürtünmə əmsalı
Əla elektrik performansı
Yanmaz
Qeyri-toksik
Tətbiqlər:
laboratoriya
Kimyəvi proses
Analiz və texnoloji avadanlıq
Emissiya monitorinqi
Aşağı temperatur
yüksək temperatur
Elektrik
ozon
PTFE molekullarının quruluşu
Politetrafloroetilen (PTFE) bir çox tetrafluoroetilen molekullarının polimerləşməsi ilə hazırlanır.
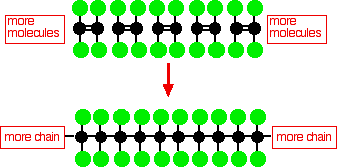
Bu sadə PTFE diaqramı molekulun üçölçülü quruluşunu göstərmir.Daha sadə molekulyar poli(etilen), molekulun karbon onurğası yalnız hidrogen atomları ilə bağlanır və bu zəncir çox çevikdir - qətiliklə xətti molekul deyil.
Bununla belə, politetrafloroetilendə CF2 qrupundakı flüor atomu bitişik qrupdakı flüor atomuna müdaxilə edəcək qədər böyükdür.Yadda saxlamaq lazımdır ki, hər flüor atomunda 3 cüt tək elektron var
Bunun təsiri karbon-karbon tək bağının fırlanmasını boğmaqdır.Flüor atomları, qonşu flüor atomlarından mümkün qədər uzaqda yerləşməyə meyllidirlər.Fırlanma qonşu karbon atomlarında flüor atomları arasında tək-cüt toqquşmaları əhatə edir ki, bu da fırlanmanı enerji baxımından əlverişsiz edir.
İtirmə qüvvəsi molekulu çubuq şəklinə salır və flüor atomları çox yumşaq bir spiral şəklində düzülür - flüor atomları karbon onurğası ətrafında spiral şəklində düzülür.Bu qurğuşun zolaqları bir qutuda uzun, nazik qələmlər kimi sıxılacaq
Bu yaxın təmas quruluşu, görəcəyiniz kimi, molekullararası qüvvələrə mühüm təsir göstərir
Molekullararası qüvvələr və PTFE-nin ərimə nöqtəsi
Politetrafloroetilenin ərimə nöqtəsi 327°C-dir.Bu, bu polimer üçün olduqca yüksəkdir, ona görə də molekullar arasında əhəmiyyətli van der Waals qüvvələri olmalıdır.
Niyə insanlar PTFE-dəki van der Waals qüvvələrinin zəif olduğunu iddia edirlər?
Van der Waals dispersiya qüvvəsi molekuldakı elektronların hərəkəti zamanı yaranan müvəqqəti dalğalanan dipollardan qaynaqlanır.PTFE molekulu böyük olduğundan, böyük bir dispersiya qüvvəsi gözləmək olardı, çünki hərəkət edə bilən çoxlu elektronlar var.
Ümumi vəziyyət ondan ibarətdir ki, molekul nə qədər böyükdürsə, dispersiya gücü də bir o qədər böyükdür
Bununla belə, PTFE-nin problemi var.Flüor çox elektronmənfidir.O, karbon-flüor bağındakı elektronları bir-birinə o qədər sıx bağlamağa meyllidir ki, elektronlar düşündüyünüz kimi hərəkət edə bilməz.Biz karbon-flüor bağını güclü qütbləşməyə malik olmayan kimi təsvir edirik
Van der Waals qüvvələrinə dipol-dipol qarşılıqlı təsirləri də daxildir.Lakin politetrafloroetilendə (PTFE) hər bir molekul bir qədər mənfi yüklü flüor atomlarının təbəqəsi ilə əhatə olunmuşdur.Bu halda molekullar arasında yeganə mümkün qarşılıqlı təsir qarşılıqlı itələmədir!
Beləliklə, dispersiya qüvvəsi düşündüyünüzdən daha zəifdir və dipol-dipol qarşılıqlı təsiri itələnməyə səbəb olacaqdır.Təəccüblü deyil ki, insanlar PTFE-də van der Waals qüvvəsinin çox zəif olduğunu söyləyirlər.Siz əslində itələyici qüvvə əldə etməyəcəksiniz, çünki dispersiya qüvvəsinin təsiri dipol-dipol qarşılıqlı təsirindən daha böyükdür, lakin xalis təsir ondan ibarətdir ki, van der Waals qüvvəsi zəifləməyə meyllidir.
Lakin PTFE çox yüksək ərimə nöqtəsinə malikdir, ona görə də molekulları bir yerdə saxlayan qüvvə çox güclü olmalıdır.
PTFE necə yüksək ərimə nöqtəsinə sahib ola bilər?
PTFE çox kristaldir, bu mənada böyük bir sahə var, molekullar çox nizamlı düzülüşdədir.Unutmayın, PTFE molekulları uzunsov çubuqlar kimi düşünülə bilər.Bu dirəklər bir-birinə sıx şəkildə yığılacaq
Bu o deməkdir ki, ptfe molekulu həqiqətən böyük müvəqqəti dipollar əmələ gətirə bilməsə də, dipollardan çox səmərəli istifadə oluna bilər.
Beləliklə, PTFE-dəki van der Waals qüvvələri zəif və ya güclüdür?
Düşünürəm ki, ikiniz də haqlı ola bilərsiniz!Politetrafloroetilen (PTFE) zəncirləri zəncirlər arasında çox sıx təmas olmayacaq şəkildə düzülürsə, aralarındakı qüvvə çox zəif olacaq və ərimə nöqtəsi çox aşağı olacaq.
Ancaq real dünyada molekullar sıx təmasdadır.Van der Waals qüvvələri ola bildikləri qədər güclü olmaya bilər, lakin PTFE-nin quruluşu onların ən böyük təsiri hiss etməsi, ümumi güclü molekullararası bağlar və yüksək ərimə nöqtələri meydana gətirməsi deməkdir.
Bu, digər qüvvələrdən fərqlidir, məsələn, dipol-dipol qarşılıqlı təsir qüvvəsi yalnız 23 dəfə və ya iki dəfə məsafə 8 dəfə azalır.
Buna görə də, PTFE-də çubuqşəkilli molekulların sıx şəkildə qablaşdırılması dispersiyanın effektivliyini artırır.
Yapışmayan xüsusiyyətlər
Buna görə su və yağ PTFE-nin səthinə yapışmır və yumurtaları tavaya yapışmadan PTFE ilə örtülmüş tavada qızartmaq olar.
Səthində digər molekulları hansı qüvvələrin sabitləyəcəyini düşünmək lazımdırPTFE.Buraya bir növ kimyəvi bağ, van der Waals qüvvəsi və ya hidrogen bağı daxil ola bilər
Kimyəvi birləşmə
Karbon-flüor bağı çox güclüdür və başqa molekulların karbon zəncirinə çatması hər hansı bir əvəzetmə reaksiyasına səbəb ola bilməz.Kimyəvi bağın meydana gəlməsi qeyri-mümkündür
van der Waals qüvvələri
Biz gördük ki, PTFE-də van der Waals qüvvəsi çox güclü deyil və bu, yalnız PTFE-nin yüksək ərimə nöqtəsinə sahib olmasına səbəb olacaq, çünki molekullar çox yaxındır və çox təsirli təmasdadırlar.
Lakin PTFE səthinə yaxın olan digər molekullar üçün bu fərqlidir.Nisbətən kiçik molekullar (məsələn, su molekulları və ya neft molekulları) səthlə yalnız az miqdarda təmasda olacaq və yalnız az miqdarda van der Waals cazibəsi yaranacaq.
Böyük bir molekul (məsələn, bir zülal) çubuq şəklində olmayacaq, ona görə də PTFE-nin aşağı qütbləşmə meylini aradan qaldırmaq üçün onunla səth arasında kifayət qədər təsirli əlaqə yoxdur.
İstənilən halda, PTFE-nin səthi ilə ətrafdakı şeylər arasında van der Waals qüvvəsi kiçik və təsirsizdir.
Hidrogen bağları
Səthdəki PTFE molekulları tamamilə flüor atomları ilə sarılır.Bu flüor atomları çox elektronegativdir, ona görə də onların hamısı müəyyən dərəcədə mənfi yük daşıyırlar.Hər bir flüor da 3 cüt çıxıntılı tək elektrona malikdir
Flüor üzərindəki tək cüt və sudakı hidrogen atomu kimi hidrogen bağlarının əmələ gəlməsi üçün lazım olan şərtlər bunlardır.Ancaq bu, açıq şəkildə baş verməyəcək, əks halda PTFE molekulları ilə su molekulları arasında güclü bir cazibə olacaq və su PTFE-yə yapışacaq.
Xülasə
Digər molekulların PTFE səthinə müvəffəqiyyətlə yapışmasının effektiv yolu yoxdur, buna görə də yapışmayan bir səthə malikdir.
Aşağı sürtünmə
PTFE-nin sürtünmə əmsalı çox aşağıdır.Bu o deməkdir ki, ptfe ilə örtülmüş bir səthiniz varsa, digər əşyalar asanlıqla onun üzərinə sürüşəcək.
Aşağıda baş verənlərin qısa xülasəsi verilmişdir.Bu, 1992-ci ildə "Politetrafloroetilenin Sürtünməsi və Aşınması" adlı məqalədən gəlir.
Sürüşmənin başlanğıcında PTFE səthi qırılır və kütlə sürüşdüyü yerə köçürülür.Bu, PTFE səthinin aşınması deməkdir.
Sürüşmə davam etdikcə bloklar nazik filmlərə çevrildi.
Eyni zamanda, mütəşəkkil bir təbəqə yaratmaq üçün PTFE-nin səthi çıxarılır.
İndi təmasda olan hər iki səth bir-birinin üzərində sürüşə bilən yaxşı təşkil edilmiş PTFE molekullarına malikdir.
Yuxarıda göstərilənlər politetrafloroetilenin tətbiqidir, politetrafloroetilen müxtəlif məhsullara çevrilə bilər, biz ptfe boru istehsalında ixtisaslaşmışıq.ptfe şlanq istehsalçıları, bizimlə ünsiyyətə xoş gəlmisiniz
ptfe hortumu ilə əlaqəli axtarışlar:
Göndərmə vaxtı: 05 may 2021-ci il





