Polytetrafluoroethylen (Polytetrafluoroethylene) ass wahrscheinlech dee meescht verbreete Fluoropolymer well et verschidde Charakteristiken huet, déi et en idealt Material fir eng breet Palette vun Uwendungen maachen.Et ass méi flexibel wéi aner ähnlech Päifen a ka bal all industriell Chemikalien widderstoen
D'Temperaturbereich ass ongeféier -330 ° F bis 500 ° F, déi de breetste Temperaturbereich ënner Fluoropolymeren ubitt.Zousätzlech huet et exzellent elektresch Eegeschaften a geréng magnetesch Permeabilitéit.Ptfe-Tubing ass déi meescht benotzt Laboratoire an Uwendungen wou chemesch Resistenz a Rengheet wesentlech sinn.PTFEhuet e ganz nidderegen Reibungskoeffizient an ass ee vun de bekanntste "Rutsch" Substanzen
Eegeschaften:
100% pure PTFE Harz
Am Verglach mat FEP, PFA, HP PFA, UHP PFA, ETFE, ECTFE, déi flexibelste Fluorpolymerleitungen
Chemesch inert, resistent géint bal all industriell Chemikalien a Léisungsmëttelen
Breet Temperaturbereich
Niddereg Pénétratioun
Glat Non-Stick Surface Finish
Niddregsten Reiwungskoeffizient
Excellent elektresch Leeschtung
Net brennbar
Net gëfteg
Uwendungen:
Labo
Chemeschen Prozess
Analyse a Prozess Ausrüstung
Emissioun Iwwerwachung
Niddreg Temperatur
héich Temperatur
Elektrizitéit
ozon
D'Struktur vun PTFE Molekülle
Polytetrafluorethylen (PTFE) gëtt duerch d'Polymeriséierung vu ville Tetrafluorethylenmoleküle gemaach
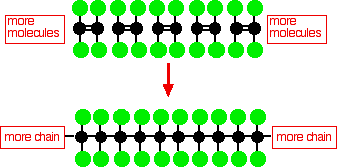
Dëst einfache PTFE Diagramm weist net déi dreidimensional Struktur vum Molekül.Am méi einfache molekulare Poly(ethylen) ass de Kuelestoff Réckgrat vun der Molekül nëmme vu Waasserstoffatome verbonnen, an dës Kette ass ganz flexibel - et ass definitiv keng linear Molekül
Wéi och ëmmer, am Polytetrafluorethylen ass de Fluoratom an enger CF2 Grupp grouss genuch fir mam Fluoratom op der benachbarer Grupp ze stéieren.Dir musst drun erënneren datt all Fluoratom 3 Puer eenzeg Elektronen huet, déi eraushänken
Den Effekt vun dësem ass d'Rotatioun vun der Kuelestoff-Kuelestoff Eenzelbindung z'ënnerdrécken.D'Fluoratome tendéieren sou arrangéiert ze sinn fir sou wäit wéi méiglech vun den ugrenzend Fluoratome ewech ze sinn.D'Rotatioun tendéiert zu Lone-Pair Kollisiounen tëscht Fluoratome op ugrenzend Kuelestoffatome involvéieren - wat d'Rotatioun energesch ongënschteg mécht
D'repulsive Kraaft gespaart d'Molekül an eng Staangform, an d'Fluoratome sinn an enger ganz sanfter Spiral arrangéiert - d'Fluoratome sinn an enger Spiral ëm de Kuelestoff-Réckgrat arrangéiert.Dës Bläistreifen wäerte wéi laang, dënn Bläistëfter an enger Këscht zesummegedréckt ginn
Dës enke Kontaktarrangement huet e wichtegen Afloss op déi intermolekulär Kräfte, wéi Dir wäert gesinn
Intermolekulär Kräften an de Schmelzpunkt vun PTFE
De Schmelzpunkt vu Polytetrafluorethylen gëtt als 327 °C zitéiert.Dëst ass zimmlech héich fir dëse Polymer, sou datt et bedeitend Van der Waals Kräfte tëscht de Moleküle musse sinn
Firwat behaapten d'Leit datt d'van der Waals Kräften am PTFE schwaach sinn?
D'Van der Waals Dispersiounskraaft gëtt verursaacht duerch déi temporär fluktuéierend Dipole generéiert wann d'Elektronen an der Molekül ronderëm bewegen.Well d'PTFE-Molekül grouss ass, géift Dir eng grouss Dispersiounskraaft erwaarden, well et vill Elektronen sinn déi sech kënne beweegen
Déi allgemeng Situatioun ass datt wat méi grouss d'Molekül ass, wat d'Dispersiounskraaft méi grouss ass
Wéi och ëmmer, PTFE huet e Problem.Fluor ass ganz elektronegativ.Et tendéiert d'Elektronen an der Kuelestoff-Fluor-Bindung enk zesummen ze binden, sou enk datt d'Elektronen net kënne beweegen wéi Dir denkt.Mir beschreiwen d'Kuelestoff-Fluorbindung als keng staark Polariséierung
Van der Waals Kräften enthalen och Dipol-Dipol Interaktiounen.Awer am Polytetrafluorethylen (PTFE) ass all Molekül vun enger Schicht vu liicht negativ gelueden Fluoratome ëmgi.An dësem Fall ass déi eenzeg méiglech Interaktioun tëscht Molekülle géigesäitege Ofstoung!
Also ass d'Dispersiounskraaft méi schwaach wéi Dir denkt, an d'Dipol-Dipol-Interaktioun verursaacht Ofstouss.Kee Wonner datt d'Leit soen datt d'Van der Waals Kraaft am PTFE ganz schwaach ass.Dir kritt tatsächlech net déi repulsiv Kraaft, well den Afloss vun der Dispersiounskraaft méi grouss ass wéi dee vun der Dipol-Dipol Interaktioun, awer den Nettoeffekt ass datt d'Van der Waals Kraaft tendéiert ze schwächen
Awer PTFE huet e ganz héije Schmelzpunkt, sou datt d'Kraaft déi d'Moleküle zesumme hält muss ganz staark sinn
Wéi kann PTFE en héije Schmelzpunkt hunn?
PTFE ass ganz kristallin, an dësem Sënn gëtt et e grousst Gebitt, d'Moleküle sinn an enger ganz regulärer Arrangement.Denkt drun, PTFE Molekülle kënnen als verlängert Staang geduecht ginn.Dës Pole wäerten enk zesummegefaasst ginn
Dëst bedeit datt obwuel d'ptfe Molekül net wierklech grouss temporär Dipole produzéiere kann, kënnen d'Dipole ganz effizient benotzt ginn
Also sinn d'van der Waals Kräften am PTFE schwaach oder staark?
Ech mengen Dir kënnt souwuel Recht hunn!Wann d'Polytetrafluorethylene (PTFE) Ketten esou arrangéiert sinn datt et net ze enke Kontakt tëscht de Ketten ass, ass d'Kraaft tëscht hinnen ganz schwaach an de Schmelzpunkt ass ganz niddereg
Awer an der realer Welt sinn d'Moleküle an enke Kontakt.Van der Waals Kräfte sinn vläicht net sou mächteg wéi se kënne sinn, awer d'Struktur vum PTFE bedeit datt se de gréissten Effekt fillen, allgemeng staark intermolekulär Bindungen an héich Schmelzpunkte produzéieren
Dëst am Géigesaz zu anere Kräften, wéi zum Beispill d'Dipol-Dipol-Interaktiounskraaft, déi nëmmen ëm 23 Mol reduzéiert gëtt, oder zweemol d'Distanz ëm 8 Mol reduzéiert gëtt
Dofir maximéiert déi enk Verpackung vu staaffërmege Molekülen am PTFE d'Effizienz vun der Dispersioun
D'Non-Stick Eegeschafte
Dofir halen d'Waasser an d'Ueleg net un d'Uewerfläch vum PTFE fest, a firwat Dir Eeër an enger PTFE-beschichteter Pan fritéiere kënnt ouni un d'Pan ze halen
Dir musst betruecht wat Kräften aner Molekülle op der Uewerfläch fix kéintPTFE.Et kann eng Aart vu chemescher Bindung enthalen, Van der Waals Kraaft oder Waasserstoffbindung
Chemesch Verbindung
D'Kuelestoff-Fluor-Bindung ass ganz staark, an et ass onméiglech fir all aner Moleküle d'Kuelestoffkette z'erreechen fir datt eng Substitutiounsreaktioun stattfënnt.Et ass onméiglech fir eng chemesch Bindung ze geschéien
van der Waals Kräften
Mir hu gesinn datt d'Van der Waals Kraaft am PTFE net ganz staark ass, an et wäert nëmmen PTFE en héije Schmelzpunkt maachen, well d'Moleküle sou no sinn datt se e ganz effektive Kontakt hunn.
Awer et ass anescht fir aner Molekülen no bei der Uewerfläch vum PTFE.Relativ kleng Molekülle (wéi Waassermoleküle oder Uelegmoleküle) wäerten nëmmen e klenge Kontakt mat der Uewerfläch hunn, an nëmmen eng kleng Quantitéit vun der Van der Waals Attraktioun gëtt generéiert.
E grousst Molekül (wéi e Protein) wäert net staangfërmeg sinn, sou datt et net genuch effektiv Kontakt tëscht him an der Uewerfläch ass fir déi geréng Polariséierungstendegkeet vu PTFE ze iwwerwannen.
Egal wéi, d'Van der Waals Kraaft tëscht der Uewerfläch vum PTFE an den Ëmgéigend ass kleng an ineffektiv
Waasserstoff Obligatiounen
D'PTFE-Moleküle op der Uewerfläch si komplett vu Fluoratome gewéckelt.Dës Fluoratome si ganz elektronegativ, sou datt se all e gewësse Grad vun negativer Ladung droen.All Fluor huet och 3 Pair vun ausstehenden eenzegen Elektronen
Dëst sinn d'Konditioune fir d'Bildung vu Waasserstoffbindungen, sou wéi dat eenzegt Paar op Fluor an de Waasserstoffatom am Waasser.Awer dëst wäert selbstverständlech net geschéien, soss gëtt et eng staark Attraktioun tëscht den PTFE-Moleküle an de Waassermoleküle, an d'Waasser hält sech un d'PTFE
Resumé
Et gëtt keen effektive Wee fir aner Moleküle fir erfollegräich un d'Uewerfläch vum PTFE ze befestigen, sou datt et eng net-Stick Uewerfläch huet
Déi niddreg Reiwung
De Reibungskoeffizient vu PTFE ass ganz niddereg.Dëst bedeit datt wann Dir eng Uewerfläch mat Ptfe beschichtet hutt, aner Saachen einfach drop rutschen.
Drënner ass e séiere Resumé vun deem wat geschitt.Dëst kënnt aus engem 1992 Pabeier mam Titel "Reibung a Verschleiung vu Polytetrafluorethylen".
Am Ufank vum Rutsch brécht d'PTFE-Uewerfläch an d'Mass gëtt iwwerall wou et rutscht.Dëst bedeit datt d'PTFE Uewerfläch verschleißt.
Wéi de Rutsch weidergeet, hunn d'Blöcke sech an dënn Filmer entfalen.
Zur selwechter Zäit gëtt d'Uewerfläch vum PTFE erausgezunn fir eng organiséiert Schicht ze bilden.
Béid Flächen a Kontakt hunn elo gutt organiséiert PTFE Moleküle déi openee rutschen kënnen
Déi uewendriwwer ass d'Aféierung vu Polytetrafluorethylen, Polytetrafluorethylen kann a ville Produkter gemaach ginn, mir si spezialiséiert fir ptfe-Rouer ze maachen,ptfe Schlauch Hiersteller, wëllkomm mat eis ze kommunizéieren
Sichen am Zesummenhang mat ptfe Schlauch:
Post Zäit: Mee-05-2021





