Politetrafluoretilenas (politetrafluoretilenas) yra bene plačiausiai naudojamas fluorpolimeras, nes jis turi keletą savybių, dėl kurių jis yra ideali medžiaga įvairioms reikmėms.Jis yra lankstesnis nei kiti panašūs vamzdžiai ir gali atsispirti beveik visoms pramoninėms cheminėms medžiagoms
Temperatūros diapazonas yra maždaug nuo -330 ° F iki 500 ° F, o tai suteikia plačiausią temperatūros diapazoną tarp fluoropolimerų.Be to, jis turi puikias elektrines savybes ir mažą magnetinį laidumą.Ptfe vamzdeliai yra plačiausiai naudojami laboratoriniai vamzdeliai ir taikymas, kur būtinas cheminis atsparumas ir grynumas.PTFEturi labai mažą trinties koeficientą ir yra viena iš labiausiai „slystančių“ žinomų medžiagų
Funkcijos:
100% gryna PTFE derva
Palyginti su FEP, PFA, HP PFA, UHP PFA, ETFE, ECTFE, lanksčiausiais fluoropolimeriniais vamzdžiais
Chemiškai inertiškas, atsparus beveik visoms pramoninėms cheminėms medžiagoms ir tirpikliams
Platus temperatūros diapazonas
Mažas įsiskverbimas
Lygus nelipnus paviršiaus apdaila
Mažiausias trinties koeficientas
Puikus elektrinis veikimas
Nedegus
Ne toksiškas
Programos:
laboratorija
Cheminis procesas
Analizės ir proceso įranga
Emisijos stebėjimas
Žema temperatūra
aukštos temperatūros
Elektra
ozonas
PTFE molekulių sandara
Politetrafluoretilenas (PTFE) gaunamas polimerizuojant daugelį tetrafluoretileno molekulių
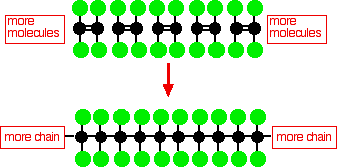
Ši paprasta PTFE diagrama neparodo trimatės molekulės struktūros.Paprastesniame molekuliniame poli(etilene) molekulės anglies stuburą jungia tik vandenilio atomai, o ši grandinė yra labai lanksti – tai tikrai nėra linijinė molekulė.
Tačiau politetrafluoretilene fluoro atomas CF2 grupėje yra pakankamai didelis, kad trukdytų gretimos grupės fluoro atomui.Turite atsiminti, kad kiekvienas fluoro atomas turi 3 poras vienišų elektronų
To poveikis yra slopinamas anglies-anglies viengubos jungties sukimasis.Fluoro atomai paprastai yra išdėstyti taip, kad būtų kuo toliau nuo gretimų fluoro atomų.Sukimasis paprastai apima pavienių porų susidūrimus tarp gretimų anglies atomų esančių fluoro atomų, todėl sukimasis yra energetiškai nepalankus.
Atstumianti jėga užfiksuoja molekulę lazdelės pavidalu, o fluoro atomai išsidėstę labai švelnia spirale – fluoro atomai išsidėstę spirale aplink anglies stuburą.Šios švino juostelės bus suspaustos kaip ilgi, ploni pieštukai dėžutėje
Kaip matysite, šis glaudus kontaktas turi didelę įtaką tarpmolekulinėms jėgoms
Tarpmolekulinės jėgos ir PTFE lydymosi temperatūra
Politetrafluoretileno lydymosi temperatūra yra 327 °C.Šis polimeras yra gana didelis, todėl tarp molekulių turi būti nemažos van der Waals jėgos
Kodėl žmonės teigia, kad van der Waals jėgos PTFE yra silpnos?
Van der Waalso dispersijos jėgą sukelia laikini svyruojantys dipoliai, susidarantys, kai molekulėje juda elektronai.Kadangi PTFE molekulė yra didelė, galite tikėtis didelės dispersijos jėgos, nes yra daug elektronų, kurie gali judėti
Bendra situacija yra tokia, kad kuo didesnė molekulė, tuo didesnė dispersijos galia
Tačiau PTFE turi problemų.Fluoras yra labai elektronegatyvus.Jis linkęs glaudžiai surišti anglies ir fluoro jungties elektronus, taip stipriai, kad elektronai negali judėti taip, kaip manote.Anglies-fluoro ryšį apibūdiname kaip neturintį stiprios poliarizacijos
Van der Waals jėgos taip pat apima dipolio ir dipolio sąveiką.Tačiau politetrafluoretilene (PTFE) kiekviena molekulė yra apsupta šiek tiek neigiamo krūvio fluoro atomų sluoksniu.Šiuo atveju vienintelė galima sąveika tarp molekulių yra abipusis atstūmimas!
Taigi dispersijos jėga yra silpnesnė, nei manote, o dipolio ir dipolio sąveika sukels atstūmimą.Nenuostabu, kad žmonės sako, kad van der Waalso jėga PTFE yra labai silpna.Jūs iš tikrųjų negausite atstūmimo jėgos, nes dispersijos jėgos įtaka yra didesnė nei dipolio ir dipolio sąveikos, tačiau grynasis poveikis yra tas, kad van der Waals jėga bus linkusi susilpnėti.
Tačiau PTFE turi labai aukštą lydymosi temperatūrą, todėl jėga, laikanti molekules kartu, turi būti labai stipri
Kaip PTFE gali turėti aukštą lydymosi temperatūrą?
PTFE yra labai kristalinis, šia prasme yra didelis plotas, molekulės yra labai taisyklingai išsidėsčiusios.Atminkite, kad PTFE molekulės gali būti laikomos pailgomis lazdelėmis.Šie poliai bus glaudžiai susitelkę
Tai reiškia, kad nors ptfe molekulė negali pagaminti tikrai didelių laikinų dipolių, dipoliai gali būti naudojami labai efektyviai.
Taigi, ar van der Waals jėgos PTFE yra silpnos ar stiprios?
Manau, kad jūs abu galite būti teisūs!Jei politetrafluoretileno (PTFE) grandinės yra išdėstytos taip, kad tarp grandinių nebūtų per glaudus kontaktas, jėga tarp jų bus labai silpna, o lydymosi temperatūra bus labai žema.
Tačiau realiame pasaulyje molekulės artimai kontaktuoja.Van der Waals jėgos gali būti ne tokios galingos, kaip gali būti, tačiau PTFE struktūra reiškia, kad jos jaučia didžiausią poveikį, sukuriant bendras stiprias tarpmolekulines jungtis ir aukštas lydymosi temperatūras.
Tai skiriasi nuo kitų jėgų, tokių kaip dipolio ir dipolio sąveikos jėga, kuri sumažinama tik 23 kartus arba du kartus atstumas sumažinamas 8 kartus
Todėl sandarus lazdelės formos molekulių įpakavimas į PTFE maksimaliai padidina dispersijos efektyvumą
Nelipnios savybės
Štai kodėl vanduo ir aliejus neprilimpa prie PTFE paviršiaus, todėl kiaušinius galite kepti PTFE dengtoje keptuvėje neprilipdami prie keptuvės.
Turite apsvarstyti, kokios jėgos gali užfiksuoti kitas molekules ant paviršiausPTFE.Tai gali apimti tam tikrą cheminę jungtį, van der Waalso jėgą arba vandenilio ryšį
Cheminis sujungimas
Anglies ir fluoro ryšys yra labai stiprus, todėl jokia kita molekulė negali pasiekti anglies grandinės, kad įvyktų pakeitimo reakcija.Neįmanoma, kad susidarytų cheminis ryšys
van der Waals pajėgos
Matėme, kad van der Waalso jėga PTFE nėra labai stipri ir dėl to PTFE bus tik aukšta lydymosi temperatūra, nes molekulės yra taip arti, kad turi labai efektyvų kontaktą.
Tačiau tai skiriasi kitoms molekulėms, esančioms arti PTFE paviršiaus.Santykinai mažos molekulės (pvz., Vandens molekulės ar aliejaus molekulės) turės tik nedidelį kontaktą su paviršiumi ir bus sukurta tik nedidelė van der Waalso trauka.
Didelė molekulė (pavyzdžiui, baltymas) nebus lazdelės formos, todėl tarp jos ir paviršiaus nėra pakankamai veiksmingo kontakto, kad būtų galima įveikti mažą PTFE poliarizacijos tendenciją.
Bet kuriuo atveju van der Waalso jėga tarp PTFE paviršiaus ir aplinkinių dalykų yra maža ir neveiksminga.
Vandenilinės jungtys
Paviršiuje esančios PTFE molekulės yra visiškai apvyniotos fluoro atomais.Šie fluoro atomai yra labai elektronegatyvūs, todėl visi jie turi tam tikrą neigiamą krūvį.Kiekvienas fluoras taip pat turi 3 poras išsikišusių vienišų elektronų
Tai sąlygos, reikalingos vandenilio ryšiams susidaryti, pavyzdžiui, vieniša pora ant fluoro ir vandenilio atomas vandenyje.Bet akivaizdu, kad tai neįvyks, kitaip tarp PTFE molekulių ir vandens molekulių bus stiprus potraukis, o vanduo prilips prie PTFE.
Santrauka
Kitoms molekulėms nėra veiksmingo būdo sėkmingai prisitvirtinti prie PTFE paviršiaus, todėl jis turi nelipnų paviršių
Maža trintis
PTFE trinties koeficientas yra labai mažas.Tai reiškia, kad jei turite paviršių, padengtą ptfe, ant jo lengvai paslys kiti dalykai.
Žemiau pateikiama trumpa to, kas vyksta, santrauka.Tai pateikta 1992 m. publikacijoje „Politetrafluoretileno trintis ir nusidėvėjimas“.
Slydimo pradžioje PTFE paviršius lūžta ir masė perkeliama ten, kur slysta.Tai reiškia, kad PTFE paviršius susidėvės.
Tęsiant slydimą, blokai išsiskleidė į plonas plėveles.
Tuo pačiu metu PTFE paviršius ištraukiamas, kad susidarytų organizuotas sluoksnis.
Dabar abu liečiantys paviršiai turi gerai organizuotas PTFE molekules, kurios gali slysti viena ant kitos
Tai yra politetrafluoretileno įvedimas, iš politetrafluoretileno galima pagaminti įvairius produktus, mes specializuojamės gaminant ptfe vamzdžius.ptfe žarnų gamintojai, kviečiame bendrauti su mumis
Paieškos, susijusios su ptfe žarna:
Paskelbimo laikas: 2021-05-05





