Politetrafluoretilēns (politetrafluoretilēns), iespējams, ir visplašāk izmantotais fluorpolimērs, jo tam ir vairākas īpašības, kas padara to par ideālu materiālu plašam lietojumu klāstam.Tas ir elastīgāks nekā citas līdzīgas caurules un var izturēt gandrīz visas rūpnieciskās ķīmiskās vielas
Temperatūras diapazons ir aptuveni no -330 ° F līdz 500 ° F, nodrošinot visplašāko temperatūras diapazonu starp fluorpolimēriem.Turklāt tam ir lieliskas elektriskās īpašības un zema magnētiskā caurlaidība.Ptfe caurules ir visplašāk izmantotās laboratorijas caurules un lietojumi, kur būtiska ir ķīmiskā izturība un tīrība.PTFEir ļoti zems berzes koeficients, un tā ir viena no visvairāk zināmajām "slīdošajām" vielām
Iespējas:
100% tīri PTFE sveķi
Salīdzinot ar FEP, PFA, HP PFA, UHP PFA, ETFE, ECTFE, elastīgākajām fluorpolimēru caurulēm
Ķīmiski inerts, izturīgs pret gandrīz visām rūpnieciskajām ķimikālijām un šķīdinātājiem
Plašs temperatūras diapazons
Zema iespiešanās
Gluda nepiedegoša virsmas apdare
Zemākais berzes koeficients
Lieliska elektriskā veiktspēja
Nedegošs
Nav toksisks
Lietojumprogrammas:
laboratorija
Ķīmiskais process
Analīzes un procesu iekārtas
Emisiju monitorings
Zema temperatūra
paaugstināta temperatūra
Elektrība
ozons
PTFE molekulu struktūra
Politetrafluoretilēnu (PTFE) iegūst, polimerizējot daudzas tetrafluoretilēna molekulas
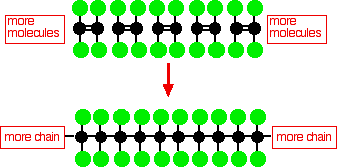
Šī vienkāršā PTFE diagramma neparāda molekulas trīsdimensiju struktūru.Vienkāršākā molekulārajā poli(etilēnā) molekulas oglekļa mugurkaulu savieno tikai ūdeņraža atomi, un šī ķēde ir ļoti elastīga - tā noteikti nav lineāra molekula.
Tomēr politetrafluoretilēnā fluora atoms CF2 grupā ir pietiekami liels, lai traucētu blakus esošās grupas fluora atomam.Jāatceras, ka katram fluora atomam ir 3 vientuļo elektronu pāri
Tā rezultātā tiek nomākta oglekļa-oglekļa vienotās saites rotācija.Fluora atomi mēdz būt izvietoti tā, lai tie būtu pēc iespējas tālāk no blakus esošajiem fluora atomiem.Rotācija mēdz būt saistīta ar atsevišķu pāru sadursmēm starp fluora atomiem uz blakus esošajiem oglekļa atomiem, kas padara rotāciju enerģētiski nelabvēlīgu
Atgrūšanas spēks nofiksē molekulu stieņa formā, un fluora atomi ir izkārtoti ļoti maigā spirālē — fluora atomi ir izkārtoti spirālē ap oglekļa mugurkaulu.Šīs svina sloksnes tiks saspiestas kopā kā gari, plāni zīmuļi kastītē
Kā jūs redzēsiet, šim ciešajam kontaktam ir liela ietekme uz starpmolekulāriem spēkiem
Starpmolekulārie spēki un PTFE kušanas temperatūra
Politetrafluoretilēna kušanas temperatūra ir norādīta kā 327 ° C.Šim polimēram tas ir diezgan augsts, tāpēc starp molekulām jābūt ievērojamiem van der Vālsa spēkiem
Kāpēc cilvēki apgalvo, ka van der Vālsa spēki PTFE ir vāji?
Van der Vāla dispersijas spēku izraisa īslaicīgi svārstīgi dipoli, kas rodas, pārvietojoties molekulā esošajiem elektroniem.Tā kā PTFE molekula ir liela, jūs varētu sagaidīt lielu izkliedes spēku, jo ir daudz elektronu, kas var pārvietoties
Vispārējā situācija ir tāda, ka jo lielāka ir molekula, jo lielāka ir dispersijas jauda
Tomēr PTFE ir problēma.Fluors ir ļoti elektronnegatīvs.Tam ir tendence cieši saistīt elektronus oglekļa-fluora saitē, tik cieši, ka elektroni nevar kustēties, kā jūs domājat.Mēs raksturojam oglekļa-fluora saiti kā bez spēcīgas polarizācijas
Van der Vālsa spēki ietver arī dipola-dipola mijiedarbību.Bet politetrafluoretilēnā (PTFE) katru molekulu ieskauj nedaudz negatīvi lādētu fluora atomu slānis.Šajā gadījumā vienīgā iespējamā mijiedarbība starp molekulām ir savstarpēja atgrūšanās!
Tātad izkliedes spēks ir vājāks, nekā jūs domājat, un dipola-dipola mijiedarbība izraisīs atgrūšanos.Nav brīnums, ka cilvēki saka, ka van der Vālsa spēks PTFE ir ļoti vājš.Jūs faktiski neiegūsit atgrūšanas spēku, jo izkliedes spēka ietekme ir lielāka nekā dipola-dipola mijiedarbības ietekme, bet neto efekts ir tāds, ka van der Vālsa spēkam ir tendence vājināties.
Bet PTFE ir ļoti augsts kušanas punkts, tāpēc spēkam, kas satur molekulas kopā, jābūt ļoti spēcīgam
Kā PTFE var būt augsts kušanas punkts?
PTFE ir ļoti kristālisks, šajā ziņā ir liels laukums, molekulas ir ļoti regulārā izkārtojumā.Atcerieties, ka PTFE molekulas var uzskatīt par iegareniem stieņiem.Šie stabi būs cieši apvienoti kopā
Tas nozīmē, ka, lai gan ptfe molekula nevar radīt patiešām lielus pagaidu dipolus, dipolus var izmantot ļoti efektīvi
Tātad, vai van der Vālsa spēki PTFE ir vāji vai spēcīgi?
Es domāju, ka jums abiem var būt taisnība!Ja politetrafluoretilēna (PTFE) ķēdes ir sakārtotas tā, lai starp ķēdēm nebūtu pārāk ciešs kontakts, spēks starp tām būs ļoti vājš un kušanas temperatūra būs ļoti zema.
Bet reālajā pasaulē molekulas ir ciešā saskarē.Van der Vālsa spēki var nebūt tik spēcīgi, kā tie varētu būt, bet PTFE struktūra nozīmē, ka tie jūt vislielāko efektu, veidojot kopumā spēcīgas starpmolekulāras saites un augstu kušanas temperatūru.
Tas ir pretstatā citiem spēkiem, piemēram, dipola-dipola mijiedarbības spēkam, kas tiek samazināts tikai 23 reizes vai divreiz attālums tiek samazināts 8 reizes.
Tāpēc stieņa formas molekulu blīvais iesaiņojums PTFE palielina dispersijas efektivitāti
Nepiedeguma īpašības
Tāpēc ūdens un eļļa nepielīp pie PTFE virsmas, un olas var cept pannā, kas pārklāta ar PTFE, nepielīpjot pie pannas.
Jums jāapsver, kādi spēki var fiksēt citas molekulas uz virsmasPTFE.Tas var ietvert kādu ķīmisko saiti, van der Vālsa spēku vai ūdeņraža saiti
Ķīmiskā saistīšana
Oglekļa-fluora saite ir ļoti spēcīga, un nav iespējams nevienai citai molekulai sasniegt oglekļa ķēdi, lai izraisītu aizvietošanas reakciju.Ķīmiskās saites veidošanās nav iespējama
van der Vālsa spēki
Mēs esam redzējuši, ka van der Vālsa spēks PTFE nav ļoti spēcīgs, un tas tikai padarīs PTFE ar augstu kušanas temperatūru, jo molekulas ir tik tuvu, ka tām ir ļoti efektīvs kontakts.
Bet tas atšķiras citām molekulām, kas atrodas tuvu PTFE virsmai.Salīdzinoši mazām molekulām (piemēram, ūdens molekulām vai eļļas molekulām) būs tikai neliels kontakts ar virsmu, un tiks radīts tikai neliels daudzums van der Vāla pievilcības.
Liela molekula (piemēram, proteīns) nebūs stieņa formas, tāpēc starp to un virsmu nav pietiekami daudz efektīva kontakta, lai pārvarētu PTFE zemo polarizācijas tendenci.
Jebkurā gadījumā van der Vālsa spēks starp PTFE virsmu un apkārtējām lietām ir mazs un neefektīvs.
Ūdeņraža saites
PTFE molekulas uz virsmas ir pilnībā iesaiņotas ar fluora atomiem.Šie fluora atomi ir ļoti elektronnegatīvi, tāpēc tiem visiem ir noteikta negatīva lādiņa pakāpe.Katram fluoram ir arī 3 pāri izvirzītu vientuļo elektronu
Šie ir apstākļi, kas nepieciešami ūdeņraža saišu veidošanai, piemēram, vientuļais pāris uz fluora un ūdeņraža atoms ūdenī.Bet tas acīmredzot nenotiks, pretējā gadījumā starp PTFE molekulām un ūdens molekulām būs spēcīga pievilcība, un ūdens pielips PTFE.
Kopsavilkums
Citām molekulām nav efektīvs veids, kā veiksmīgi piestiprināties pie PTFE virsmas, tāpēc tam ir nepiedegoša virsma.
Zemā berze
PTFE berzes koeficients ir ļoti zems.Tas nozīmē, ka, ja jums ir virsma, kas pārklāta ar ptfe, uz tās viegli paslīdēs citas lietas.
Tālāk ir sniegts īss notiekošā kopsavilkums.Tas nāk no 1992. gada dokumenta ar nosaukumu "Politetrafluoretilēna berze un nodilums".
Slīdēšanas sākumā PTFE virsma saplīst un masa tiek pārnesta uz jebkuru vietu, kur tā slīd.Tas nozīmē, ka PTFE virsma nolietosies.
Slīdēšanai turpinoties, bloki izvērtās plānās plēvēs.
Tajā pašā laikā PTFE virsma tiek izvilkta, veidojot organizētu slāni.
Abām saskares virsmām tagad ir labi sakārtotas PTFE molekulas, kas var slīdēt viena uz otru
Iepriekš minētais ir politetrafluoretilēna ieviešana, politetrafluoretilēnu var izgatavot dažādos produktos, mēs specializējamies ptfe cauruļu ražošanā.ptfe šļūteņu ražotāji, laipni lūdzam sazināties ar mums
Ar ptfe šļūteni saistītie meklējumi:
Izlikšanas laiks: 05.05.2021





