Политетрафлуороетилен (политетрафлуороетилен) е веројатно најкористениот флуорополимер бидејќи има неколку карактеристики што го прават идеален материјал за широк опсег на апликации.Тој е пофлексибилен од другите слични цевки и може да одолее на речиси сите индустриски хемикалии
Температурниот опсег е приближно -330°F до 500°F, обезбедувајќи најширок температурен опсег меѓу флуорополимерите.Покрај тоа, има одлични електрични својства и мала магнетна пропустливост.Ptfe цевките се најшироко користените лабораториски цевки и апликации каде хемиската отпорност и чистота се неопходни.Тефлонскиима многу низок коефициент на триење и е една од најпознатите „лизгачки“ супстанции
Карактеристики:
100% чиста тефлонска смола
Во споредба со FEP, PFA, HP PFA, UHP PFA, ETFE, ECTFE, најфлексибилните флуорополимерни цевки
Хемиски инертен, отпорен на речиси сите индустриски хемикалии и растворувачи
Широк температурен опсег
Ниска пенетрација
Мазна нелеплива завршница на површината
Најнизок коефициент на триење
Одлични електрични перформанси
Не запаливо
Нетоксични
Апликации:
лабораторија
Хемиски процес
Анализа и процесна опрема
Мониторинг на емисиите
Ниска температура
висока температура
Електрична енергија
озонот
Структурата на тефлонските молекули
Политетрафлуороетилен (PTFE) е направен со полимеризација на многу тетрафлуороетиленски молекули
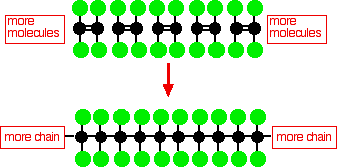
Овој едноставен тефлонски дијаграм не ја покажува тродимензионалната структура на молекулата.Во поедноставниот молекуларен поли(етилен), јаглеродниот 'рбет на молекулата е поврзан само со атоми на водород, а овој ланец е многу флексибилен - дефинитивно не е линеарна молекула
Меѓутоа, во политетрафлуороетилен, атомот на флуор во групата CF2 е доволно голем за да се меша со атомот на флуор на соседната група.Мора да запомните дека секој атом на флуор има 3 пара осамени електрони кои се штрчат
Ефектот од ова е да се потисне ротацијата на единечната врска јаглерод-јаглерод.Атомите на флуор имаат тенденција да бидат наредени така што да бидат што подалеку од соседните атоми на флуор.Ротацијата има тенденција да вклучува судири од еден пар помеѓу атоми на флуор на соседните јаглеродни атоми - што ја прави ротацијата енергетски неповолна
Одбивната сила ја заклучува молекулата во форма на прачка, а атомите на флуор се наредени во многу нежна спирала - атомите на флуор се наредени во спирала околу јаглеродниот 'рбет.Овие оловни ленти ќе бидат стиснати заедно како долги, тенки моливи во кутија
Овој близок контакт аранжман има важно влијание врз меѓумолекуларните сили, како што ќе видите
Меѓумолекуларни сили и точка на топење на тефлонски
Точката на топење на политетрафлуороетилен е цитирана како 327°C.Ова е доста високо за овој полимер, така што мора да има значителни ван дер Валс сили помеѓу молекулите
Зошто луѓето тврдат дека силите на ван дер Валс во тефлонски се слаби?
Ван дер Валсовата дисперзивна сила е предизвикана од привремените флуктуирачки диполи генерирани кога електроните во молекулата се движат наоколу.Бидејќи тефлонската молекула е голема, би очекувале голема дисперзивна сила бидејќи има многу електрони кои можат да се движат
Општата ситуација е дека колку е поголема молекулата, толку е поголема моќта на дисперзија
Сепак, тефлонскиот има проблем.Флуорот е многу електронегативен.Тој има тенденција цврсто да ги врзува електроните во врската јаглерод-флуор, толку цврсто што електроните не можат да се движат како што мислите.Ја опишуваме врската јаглерод-флуор дека нема силна поларизација
Силите на Ван дер Валс, исто така, вклучуваат интеракции дипол-дипол.Но, во политетрафлуороетилен (PTFE), секоја молекула е опкружена со слој од малку негативно наелектризирани атоми на флуор.Во овој случај, единствената можна интеракција помеѓу молекулите е меѓусебното одбивање!
Така, силата на дисперзија е послаба отколку што мислите, а интеракцијата дипол-дипол ќе предизвика одбивност.Не е ни чудо што луѓето велат дека силата на ван дер Валс во тефлонски е многу слаба.Вие всушност нема да ја добиете одбивната сила, бидејќи влијанието на силата на дисперзија е поголемо од она на интеракцијата дипол-дипол, но нето ефектот е дека ван дер Валсовата сила ќе има тенденција да ослабне
Но, тефлонскиот има многу висока точка на топење, така што силата што ги држи молекулите заедно мора да биде многу силна
Како може тефлонскиот да има висока точка на топење?
Тефлонски е многу кристален, во оваа смисла има голема површина, молекулите се во многу редовен распоред.Запомнете, молекулите на тефлонски може да се сметаат како издолжени прачки.Овие столбови ќе бидат тесно групирани заедно
Ова значи дека иако молекулата на тефлонски гасови не може да произведе навистина големи привремени диполи, диполите може да се користат многу ефикасно
Значи, дали силите на ван дер Валс во тефлонски се слаби или силни?
Мислам дека и двајцата можете да бидете во право!Ако синџирите од политетрафлуороетилен (тефлонски) се наредени на таков начин што нема премногу близок контакт помеѓу синџирите, силата меѓу нив ќе биде многу слаба, а точката на топење ќе биде многу мала.
Но, во реалниот свет, молекулите се во близок контакт.Силите на Ван дер Валс можеби не се толку моќни како што може да бидат, но структурата на тефлонски значи дека тие го чувствуваат најголемиот ефект, создавајќи севкупни силни меѓумолекуларни врски и високи точки на топење
Ова е за разлика од другите сили, како што е силата на интеракција дипол-дипол, која е намалена само за 23 пати, или двојно од растојанието е намалена за 8 пати
Затоа, тесното пакување на молекули во облик на прачка во тефлонски ја максимизира ефикасноста на дисперзијата
Нелепливи својства
Ова е причината зошто водата и маслото не се лепат на површината на тефлонски и зошто можете да пржете јајца во тава обложена со тефлонски без да се залепат за тавата
Треба да размислите кои сили можат да ги поправат другите молекули на површината наТефлонски.Може да вклучува некаква хемиска врска, ван дер Валсова сила или водородна врска
Хемиско поврзување
Врската јаглерод-флуор е многу силна и невозможно е која било друга молекула да стигне до јаглеродниот синџир за да предизвика реакција на супституција.Невозможно е да се појави хемиска врска
силите на ван дер Валс
Видовме дека ван дер Валсовата сила во тефлонски не е многу силна и само ќе направи тефлонскиот да има висока точка на топење, бидејќи молекулите се толку блиску што имаат многу ефективен контакт.
Но, тоа е различно за другите молекули блиску до површината на тефлонски.Релативно малите молекули (како што се молекулите на водата или молекулите на маслото) ќе имаат само мала количина на контакт со површината и ќе се генерира само мала количина на ван дер Валсова привлечност.
Голема молекула (како што е протеинот) нема да биде во форма на прачка, така што нема доволно ефективен контакт помеѓу неа и површината за да се надмине тенденцијата на ниска поларизација на тефлонски.
Во секој случај, ван дер Валсовата сила помеѓу површината на тефлонскиот и околните работи е мала и неефикасна
Водородни врски
Тефлонските молекули на површината се целосно обвиткани со атоми на флуор.Овие атоми на флуор се многу електронегативни, така што сите тие носат одреден степен на негативен полнеж.Секој флуор има и 3 пара испакнати осамени електрони
Ова се условите потребни за формирање на водородни врски, како што е осамениот пар на флуор и водородниот атом во водата.Но, ова очигледно нема да се случи, инаку ќе има силна привлечност помеѓу тефлонските молекули и молекулите на водата, а водата ќе се залепи за тефлонскиот
Резиме
Не постои ефикасен начин другите молекули успешно да се закачат на површината на тефлонскиот, па затоа има нелеплива површина
Ниското триење
Коефициентот на триење на тефлонски е многу низок.Тоа значи дека ако имате површина обложена со тефлонски материјал, другите работи лесно ќе се лизгаат на неа.
Подолу е кратко резиме на она што се случува.Ова доаѓа од труд од 1992 година со наслов „Триење и абење на политетрафлуороетилен“.
На почетокот на лизгањето, тефлонската површина се кине и масата се пренесува каде и да се лизга.Ова значи дека тефлонската површина ќе се истроши.
Како што продолжуваше лизгањето, блоковите се расплетуваа во тенки филмови.
Во исто време, површината на тефлонски се извлекува за да се формира организиран слој.
И двете површини во контакт сега имаат добро организирани тефлонски молекули кои можат да се лизгаат една на друга
Горенаведеното е воведување на политетрафлуороетилен, политетрафлуороетилен може да се направи во различни производи, ние сме специјализирани за правење тефлонски цевки,производители на тефлонски црева, добредојдовте да комуницирате со нас
Пребарувања поврзани со тефлонско црево:
Време на објавување: мај-05-2021 година





