Politetrafluoroetileni (politetrafluoroetilen) është ndoshta fluoropolimeri më i përdorur sepse ka disa karakteristika që e bëjnë atë një material ideal për një gamë të gjerë aplikimesh.Është më fleksibël se tubat e tjerë të ngjashëm dhe mund t'i rezistojë pothuajse të gjitha kimikateve industriale
Gama e temperaturës është afërsisht -330°F deri në 500°F, duke siguruar gamën më të gjerë të temperaturës midis fluoropolimereve.Përveç kësaj, ka veti të shkëlqyera elektrike dhe përshkueshmëri të ulët magnetike.Tubi Ptfe është tubacioni laboratorik dhe aplikacionet më të përdorura ku rezistenca kimike dhe pastërtia janë thelbësore.PTFEka një koeficient shumë të ulët fërkimi dhe është një nga substancat më "rrëshqitëse" të njohura
Karakteristikat:
100% rrëshirë PTFE e pastër
Krahasuar me FEP, PFA, HP PFA, UHP PFA, ETFE, ECTFE, tubat më fleksibël fluoropolimer
Kimikisht inerte, rezistent ndaj pothuajse të gjitha kimikateve industriale dhe tretësve
Gama e gjerë e temperaturës
Penetrim i ulët
Finim i lëmuar i sipërfaqes që nuk ngjit
Koeficienti më i ulët i fërkimit
Performancë e shkëlqyer elektrike
Nuk merr flake
Jo toksike
Aplikimet:
laboratori
Procesi kimik
Pajisjet e analizës dhe procesit
Monitorimi i emetimeve
Temperatura e ulët
temperaturë të lartë
Elektricitet
ozonit
Struktura e molekulave PTFE
Politetrafluoroetilen (PTFE) është bërë nga polimerizimi i shumë molekulave tetrafluoroetileni
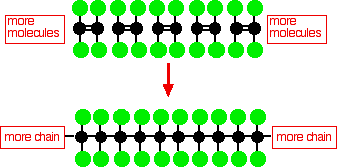
Ky diagram i thjeshtë PTFE nuk tregon strukturën tre-dimensionale të molekulës.Në polin molekular më të thjeshtë (etilen), shtylla kurrizore e karbonit të molekulës është e lidhur vetëm nga atomet e hidrogjenit, dhe ky zinxhir është shumë fleksibël - definitivisht nuk është një molekulë lineare.
Sidoqoftë, në politetrafluoroetilen, atomi i fluorit në një grup CF2 është mjaft i madh për të ndërhyrë me atomin e fluorit në grupin ngjitur.Duhet të mbani mend se çdo atom fluori ka 3 palë elektrone të vetme që dalin jashtë
Efekti i kësaj është të shtypë rrotullimin e lidhjes së vetme karbon-karbon.Atomet e fluorit priren të vendosen në mënyrë që të jenë sa më larg që të jetë e mundur nga atomet e fluorit ngjitur.Rrotullimi tenton të përfshijë përplasje të një çifti të vetëm midis atomeve të fluorit në atomet fqinje të karbonit - gjë që e bën rrotullimin energjikisht të pafavorshëm
Forca refuzuese e mbyll molekulën në një formë shufre dhe atomet e fluorit janë të rregulluar në një spirale shumë të butë - atomet e fluorit janë të rregulluar në një spirale rreth shtyllës kurrizore të karbonit.Këto shirita plumbi do të shtrydhen së bashku si lapsa të gjatë e të hollë në një kuti
Ky rregullim i ngushtë i kontaktit ka një ndikim të rëndësishëm në forcat ndërmolekulare, siç do ta shihni
Forcat ndërmolekulare dhe pika e shkrirjes së PTFE
Pika e shkrirjes së politetrafluoroetilenit është 327°C.Kjo është mjaft e lartë për këtë polimer, kështu që duhet të ketë forca të konsiderueshme van der Waals midis molekulave
Pse njerëzit pretendojnë se forcat van der Waals në PTFE janë të dobëta?
Forca e dispersionit van der Waals shkaktohet nga dipolet e përkohshme luhatëse të krijuara kur elektronet në molekulë lëvizin përreth.Për shkak se molekula PTFE është e madhe, do të prisnit një forcë të madhe dispersioni sepse ka shumë elektrone që mund të lëvizin
Situata e përgjithshme është se sa më e madhe të jetë molekula, aq më e madhe është fuqia e shpërndarjes
Megjithatë, PTFE ka një problem.Fluori është shumë elektronegativ.Ai tenton t'i lidhë elektronet në lidhjen karbon-fluor fort së bashku, aq fort sa elektronet nuk mund të lëvizin siç mendoni.Ne e përshkruajmë lidhjen karbon-fluor si pa polarizim të fortë
Forcat Van der Waals përfshijnë gjithashtu ndërveprimet dipol-dipol.Por në politetrafluoroetilen (PTFE), çdo molekulë është e rrethuar nga një shtresë e atomeve të fluorit të ngarkuar pak negativisht.Në këtë rast, ndërveprimi i vetëm i mundshëm midis molekulave është zmbrapsja e ndërsjellë!
Pra, forca e dispersionit është më e dobët nga sa mendoni, dhe ndërveprimi dipol-dipol do të shkaktojë zmbrapsje.Nuk është çudi që njerëzit thonë se forca van der Waals në PTFE është shumë e dobët.Në fakt nuk do të merrni forcën refuzuese, sepse ndikimi i forcës së dispersionit është më i madh se ai i ndërveprimit dipol-dipol, por efekti neto është se forca van der Waals do të tentojë të dobësohet.
Por PTFE ka një pikë shkrirjeje shumë të lartë, kështu që forca që mban molekulat së bashku duhet të jetë shumë e fortë
Si mund të ketë PTFE një pikë shkrirjeje të lartë?
PTFE është shumë kristalor, në këtë kuptim ka një zonë të madhe, molekulat janë në një rregullim shumë të rregullt.Mos harroni, molekulat PTFE mund të mendohen si shufra të zgjatur.Këto pole do të grumbullohen ngushtë së bashku
Kjo do të thotë se megjithëse molekula ptfe nuk mund të prodhojë dipole të përkohshme vërtet të mëdha, dipolet mund të përdoren me shumë efikasitet
Pra, a janë forcat van der Waals në PTFE të dobëta apo të forta?
Unë mendoj se të dy mund të keni të drejtë!Nëse zinxhirët e politetrafluoroetilenit (PTFE) janë rregulluar në atë mënyrë që të mos ketë kontakt shumë të ngushtë midis zinxhirëve, forca midis tyre do të jetë shumë e dobët dhe pika e shkrirjes do të jetë shumë e ulët.
Por në botën reale, molekulat janë në kontakt të ngushtë.Forcat Van der Waals mund të mos jenë aq të fuqishme sa mund të jenë, por struktura e PTFE do të thotë se ata ndjejnë efektin më të madh, duke prodhuar lidhje të përgjithshme të forta ndërmolekulare dhe pika të larta shkrirjeje
Kjo është në kontrast me forcat e tjera, të tilla si forca e ndërveprimit dipol-dipol, e cila zvogëlohet vetëm me 23 herë, ose dyfishi i distancës zvogëlohet me 8 herë.
Prandaj, paketimi i ngushtë i molekulave në formë shufre në PTFE maksimizon efektivitetin e shpërndarjes
Vetitë jo ngjitëse
Kjo është arsyeja pse uji dhe vaji nuk ngjiten në sipërfaqen e PTFE dhe pse mund të skuqni vezët në një tigan të veshur me PTFE pa u ngjitur në tigan
Ju duhet të merrni parasysh se cilat forca mund të fiksojnë molekula të tjera në sipërfaqePTFE.Mund të përfshijë një lloj lidhjeje kimike, forcë van der Waals ose lidhje hidrogjeni
Lidhja kimike
Lidhja karbon-fluor është shumë e fortë dhe është e pamundur që ndonjë molekulë tjetër të arrijë zinxhirin e karbonit për të shkaktuar një reaksion zëvendësimi.Është e pamundur që të ndodhë një lidhje kimike
forcat van der Waals
Ne kemi parë që forca van der Waals në PTFE nuk është shumë e fortë dhe vetëm do të bëjë që PTFE të ketë një pikë shkrirjeje të lartë, sepse molekulat janë aq afër sa kanë kontakt shumë efektiv.
Por është ndryshe për molekulat e tjera afër sipërfaqes së PTFE.Molekulat relativisht të vogla (të tilla si molekulat e ujit ose molekulat e vajit) do të kenë vetëm një sasi të vogël kontakti me sipërfaqen, dhe vetëm një sasi e vogël tërheqjeje van der Waals do të gjenerohet.
Një molekulë e madhe (siç është një proteinë) nuk do të jetë në formë shufre, kështu që nuk ka kontakt të mjaftueshëm efektiv midis saj dhe sipërfaqes për të kapërcyer tendencën e ulët të polarizimit të PTFE.
Sido që të jetë, forca van der Waals midis sipërfaqes së PTFE dhe gjërave përreth është e vogël dhe joefektive
Lidhjet e hidrogjenit
Molekulat PTFE në sipërfaqe janë mbështjellë plotësisht nga atomet e fluorit.Këto atome të fluorit janë shumë elektronegativë, kështu që të gjithë mbajnë një shkallë të caktuar të ngarkesës negative.Çdo fluor ka gjithashtu 3 palë elektrone të vetme të spikatura
Këto janë kushtet e nevojshme për formimin e lidhjeve hidrogjenore, të tilla si çifti i vetëm në fluor dhe atomi i hidrogjenit në ujë.Por kjo padyshim nuk do të ndodhë, përndryshe do të ketë një tërheqje të fortë midis molekulave të PTFE dhe molekulave të ujit, dhe uji do të ngjitet në PTFE
Përmbledhje
Nuk ka asnjë mënyrë efektive që molekulat e tjera të ngjiten me sukses në sipërfaqen e PTFE, kështu që ajo ka një sipërfaqe jo ngjitëse
Fërkimi i ulët
Koeficienti i fërkimit të PTFE është shumë i ulët.Kjo do të thotë që nëse keni një sipërfaqe të veshur me ptfe, gjërat e tjera do të rrëshqasin lehtësisht mbi të.
Më poshtë është një përmbledhje e shpejtë e asaj që po ndodh.Kjo vjen nga një punim i vitit 1992 me titull "Fërkimi dhe veshja e politetrafluoroetilenit".
Në fillim të rrëshqitjes sipërfaqja e PTFE thyhet dhe masa bartet kudo ku rrëshqet.Kjo do të thotë që sipërfaqja PTFE do të konsumohet.
Ndërsa rrëshqitja vazhdoi, blloqet u shpalosën në filma të hollë.
Në të njëjtën kohë, sipërfaqja e PTFE tërhiqet për të formuar një shtresë të organizuar.
Të dyja sipërfaqet në kontakt tani kanë molekula PTFE të mirëorganizuara që mund të rrëshqasin mbi njëra-tjetrën
Sa më sipër është futja e politetrafluoroetilenit, politetrafluoroetilen mund të bëhet në një shumëllojshmëri produktesh, ne jemi të specializuar në prodhimin e tubit ptfe,prodhuesit e zorrëve ptfe, të mirëpritur të komunikoni me ne
Kërkimet në lidhje me zorrën ptfe:
Koha e postimit: Maj-05-2021





